Apakah itu kanser usus besar?
Kanser Usus Besar (CRC) adalah kanser ketiga yang paling kerap di seluruh dunia selepas kanser paru-paru dan payudara. Sebanyak 1,931,590 kes baru CRC dicatatkan pada tahun 2020 dan kematian sebanyak 935 173 kes. Di Malaysia, 15,515 (13.5%) CRC kes baru yang dilaporkan dari jumlah keseluruhan 115,238 keseluruhan kanser yang dilaporkan ada dari tahun 2012 to 2016 (Rajah 1).

Sumber: Malaysian National Cancer Registry Report 2012-2016
CRC adalah paling kerap di kalangan lelaki dan kedua kerap di kalangan wanita di Malaysia. Sebilangan besar pesakit CRC adalah dari kumpulan yang lebih tua yang berusia antara 70 hingga 74 tahun. Sebanyak 36% lelaki dan 33% pesakit wanita mendapat diagnosis pada peringkat akhir yang mana sel kanser telah merebak ke organ yang lain seperti hati dan paru-paru. Kadar kelangsungan hidup pesakit CRC bergantung pada tahap kanser tersebut. Kadar kelangsungan hidup 5 tahun dinyatakan sebagai 90% untuk tahap 1, 80% untuk tahap 2, 30-60% untuk tahap 3 dan kira-kira 5-10% untuk pesakit tahap 4.
Rawatan Kanser Usus Besar
Rawatan lazim semasa untuk CRC termasuk pembedahan, kemoterapi dan terapi radiasi. Walau bagaimanapun, 30 – 40% pesakit CRC yang menjalani rawatan ini, mengalami pertumbuhan sel kanser semula dalam tempoh 5 tahun selepas didiagnosis waktu pertama kali.
Bergantung pada lokasi dan tahap barah tersebut, rawatan lazim ini dapat digunakan dalam bentuk kombinasi gabungan. Pembedahan sering menjadi pilihan sebagai rawatan pertama dan khusus untuk sel kanser yang lokasinya masih setempat, mudah dicapai dan belum merebak ke organ lain. Walau bagaimanapun, penyingkiran secara total semua sel barah secara pembedahan adalah sukar untuk dicapai. Malah, lebih kurang 66% and 61% pesakit CRC tahap II dan III perlu menjalani rawatan selanjutnya dengan kemoterapi dan / atau radioterapi. Rawatan ini walaupun berkesan, namun disebabkan kurang spesifik, menyebabkan sel-sel normal lain turut mati. Akibatnya, banyak kesan sampingan seperti keguguran rambut, muntah berterusan, cirit-birit yang kerap dan keletihan yang berpanjangan.
Alternatif rawatan yang lebih spesifik dan kurang kesan sampingan adalah sangat diperlukan untuk meningkatkan kualiti rawatan kanser. Salah satu pilihannya adalah imunoterapi sel kanser bersasar. Imunoterapi adalah rawatan biologi yang secara semula jadi dapat merangsang sistem imun pesakit secara khusus dalam mensasarkan dan membasmi sel barah dengan kesan sampingan yang lebih rendah.
Imunoterapi kanser mengatasi masalah kekhususan (spesifik) yang merupakan masalah utama dalam kemoterapi dan radioterapi. Kanser imunoterapi mensasarkan antigen khusus yang terdapat pada pada sel kanser secara khusus dengan memberi isyarat dan amaran kepada sistem pertahanan badan (imun) terhadap kehadiran bahan asing dan membasmi sel-sel kanser melalui tindak balas imun yang kompleks. Menariknya, sel normal tanpa antigen kanser tidak akan terjejas disebabkan kekhususan rawatan ini. Hasil rawatan daripada beberapa kanser imunoterapi adalah agak memberangsangkan dalam beberapa kes, namun rawatan ini sangat bergantung pada status sistem imun pesakit itu sendiri dan kos rawatan yang agak tinggi. Pesakit yang memberi tindak balas yang baik terhadap kanser imunoterapi akan mempunyai kesan jangka hayat yang lebih baik dan peningkatan dalam kualiti hidup.
Jenis-jenis kanser immunoterapi
1) Antibodi monoklonal (mAbs)

(Sumber: Johdi & Sukor, 2020)
Antigen kanser yang berkaitan dengan kanser (TAA) atau antigen khusus kanser (TSA) terdapat banyak di permukaan sel-sel kanser. Isyarat yang dihasilkan oleh aktiviti reseptor kemudian memberi isyarat kepada sel-sel imun untuk ke lokasi kanser dan menghasilkan tindak balas imun yang khusus kepada sel-sel kanser. Ini seterusnya menyebabkan kematian sel-sel kanser.
2) Perencat pusat pemeriksaan imun
Perencat pusat pemeriksaan imun adalah mAbs imunomodulator yang digunakan dalam imunoterapi kanser untuk mensasarkan dan menyekat ligan protein tertentu pada permukaan sel T atau subpopulasi sel imun yang lain. Pengikatan ini merangsang penindasan sel-sel kanser yang diperantarai oleh sel imun dan membunuh sel barah dengan berkesan. Perencat pusat pemeriksaan imun yang paling banyak dikaji adalah program PD / PDL-1 dan CTLA4 kerana keberkesanannya dalam merawat pelbagai barah pepejal dan darah.
3) Pemindahan sel adaptif (ACT)
ACT adalah sel terapi yang menggunakan sel T pesakit atau dikenali sebagai limfosit yang mengandungi reseptor antigen chimeric (CAR) untuk membunuh sel-sel kanser dengan berkesan. Pada masa ini, terdapat tiga cara untuk ACT iaitu limfosit penyusupan barah (TIL), pengubahsuaian reseptor sel T (TCR) dan penyisipan reseptor antigen chimeric (CAR).
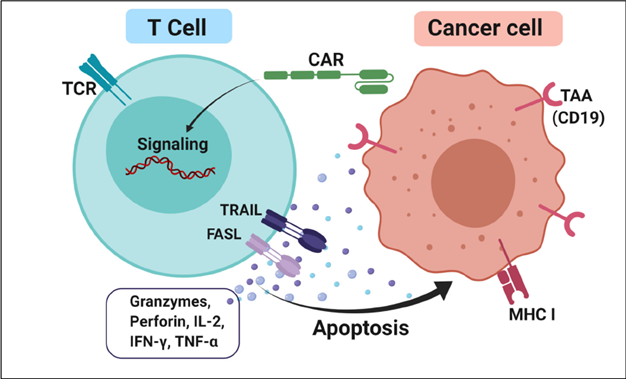
(Sumber: Johdi & Sukor, 2020)
Rujukan
1) Bray, F., Ferlay, J., Soerjomataram, I., Siegel, R. L., Torre, L. A. and Jemal, A. (2018) Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 68, 394-424. doi:10.3322/caac.21492
2) Ferlay, J., Colombet, M., Soerjomataram, I., Mathers, C., Parkin, D. M., Piñeros, M., Znaor, A. and Bray, F. (2018) Estimating the global cancer incidence and mortality in 2018: GLOBOCAN sources and methods. Int J Cancer. doi: 10.1002/ijc.31937
3) Azizah AM., Hashimah B., Nirmal K., Siti Zubaidah AR., Puteri NA., Nabihah A., Sukumaran R., Balqis B., al, e. and Nadia SMR., S. S., Rahayu O., Nur Alham O., Azlina AA. (2019) Malaysian National Cancer Registry Report 2012-2016, Malaysia Cancer Statistics, Data and Figure. National Cancer Institue.
4) Abu Hassan, M. R., Ismail, I., Mohd Suan, M. A., Ahmad, F., Wan Khazim, W. K., Othman, Z., Mat Said, R., et al. 2016. Incidence and mortality rates of colorectal cancer in Malaysia. Epidemiol Health 38: e2016007-0. doi:10.4178/epih.e2016007
5) Azizah, A. M., Nor Saleha, I. T., Noor Hashimah, A., Asmah, Z. A. & Mastulu, W. 2016. Malaysian National Cancer Registry Report 2007-2011, Malaysia Cancer Statistics, Data and Figure. National Cancer Institue 16: 203. doi:MOH/P/KN/01.16(AR).
6) Veettil, S. K., Lim, K. G., Chaiyakunapruk, N., Ching, S. M. & Abu Hassan, M. R. 2017. Colorectal cancer in Malaysia: Its burden and implications for a multiethnic country. Asian Journal of Surgery 40(6): 481–489. doi:10.1016/j.asjsur.2016.07.005.
7) Arnold M, Sierra MS, Laversanne M, Soerjomataram I, Jemal A, Bray F. Global patterns and trends in colorectal cancer incidence and mortality. Gut. (2016) 66:683–91. doi: 10.1136/gutjnl-2015-31 0912
8) Yoshino T, Arnold D, Taniguchi H, Pentheroudakis G, Yamazaki K, Xu RH, et al. Pan-Asian adapted ESMO consensus guidelines for the management of patients with metastatic colorectal cancer: A JSMO-ESMO initiative endorsed by CSCO, KACO, MOS, SSO and TOS. Ann Oncol. (2018) 29:44–70. doi: 10.1093/annonc/mdx738.
9) Park SC, Sohn DK, Kim MJ, Chang HJ, Han KS, Hyun JH, et al. Phase II clinical trial to evaluate the efficacy of transanal endoscopic total mesorectal excision for rectal cancer. Dis Colon Rectum. (2018) 61:554–60. doi: 10.1097/DCR.0000000000001058.
10) Miller KD, Nogueira L, Mariotto AB, Rowland JH, Yabroff KR, Alfano CM, et al. Cancer treatment and survivorship statistics, 2019. CA Cancer J Clin. (2019) 0:1–23. doi: 10.3322/caac.21565.
11) Seidel JA, Otsuka A, Kabashima K. Anti-PD-1 and Anti-CTLA-4 therapies in cancer: mechanisms of action, efficacy, and limitations. Front Oncol. (2018) 8:86. doi: 10.3389/fonc.2018.00086.
12) Rusch T, Bayry J, Werner J, Shevchenko I, Bazhin AV. Immunotherapy as an option for cancer treatment. Arch Immunol Ther Exp (Warsz). (2018) 66:89–96. doi: 10.1007/s00005-017-0491-5.
13) Benmebarek MR, Karches CH, Cadilha BL, Lesch S, Endres S, Kobold S. Killing mechanisms of chimeric antigen receptor (CAR) T cells. Int J Mol Sci. (2019) 20:1283. doi: 10.3390/ijms20061283
Kredit Foto : medicalindependent

